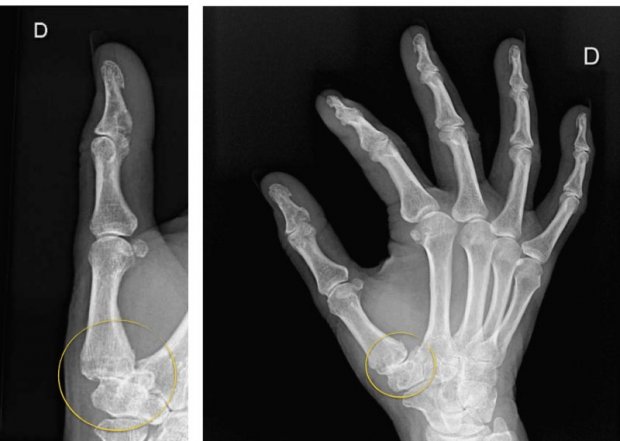
Le traitement de la rhizarthrose repose sur une prise en charge médicale et parfois un recours à une chirurgie. Ce traitement a été codifié dans des recommandations européennes, dites recommandations de l’Eular, publiées en 2007.
Les premières recommandations portent sur l’importance de la prise en charge des traitements dits non pharmacologiques.
| Lire aussi : Qu’est ce que la rhizarthrose ? |
La recommandation 3 porte sur l’intérêt des exercices qui visent à augmenter la mobilité articulaire et à préserver la force musculaire des muscles abducteur et adducteur du pouce.
La recommandation 4 porte sur l’intérêt de l’application locale de chaleur (par cire de paraffine, par pansement chauffant) notamment au cours de l’exercice physique. On peut également avoir recours aux ultrasons qui sont des traitements parfois antalgiques. Une prise en charge globale peut se faire au cours de cures thermales.
La recommandation 5 porte sur l’intérêt du port d’attelle. Il s’agit d’une attelle qui vise à immobiliser l’articulation trapézo-métacarpienne en prenant la base du pouce avec un appui jusqu’à là MP, et un appui sur le bord de l’index ainsi qu’une bande entourant le poignet. Le port de cette attelle est surtout recommandé la nuit.
L’étude de Rannou et al., menée sur 112 patients, a comparé le port d’une attelle nocturne à un traitement classique de la rhizarthrose chez des patientes symptomatiques. La compliance dans cet essai du port de l’orthèse était de plus de 80 %.
L’évaluation clinique s’est faite au premier mois puis jusqu’à un an d’évolution sur des scores de douleur et des scores de handicap. À douze mois, tous les indices concernant la douleur et le handicap favorisent le port de l’orthèse avec une différence significative par rapport au groupe n’en n’ayant pas porté.
En revanche, cette orthèse n’augmente pas à la force de préhension de la pince pouce-index. En pratique, l’adhésion des patients au port de l’attelle n’est pas toujours aussi facile à obtenir.
Traitement pharmacologique
Comme pour n’importe quelle autre articulation siège d’une arthrose, on aura bien entendu recours aux antalgiques de niveau 1, de niveau 2, en évitant la prescription d’opioïde en raison des risques inhérents à cette classe thérapeutique.
Le recours aux anti-inflammatoires est classique. Il faut privilégier, comme l’indique la recommandation européenne, le recours aux formes transcutanées d’anti-inflammatoire, voire de Capsaïsine. Ces topiques locaux ont une efficacité indéniable. On peut aussi avoir recours aux anti-inflammatoires par voie orale par des prescriptions à des doses adaptées en tenant compte des co-morbidités des patients et sur une période la plus courte possible.
Les anti-arthrosiques à action lente peuvent être prescrits même si aucune étude ne s’est intéressée spécifiquement à leur efficacité dans la rhizarthrose.
En cas d’échec de ces traitements, on peut avoir recours à des infiltrations intra-articulaires, lors des poussées douloureuses. Les infiltrations de corticoïdes font partie de la recommandation no 10 des recommandations européennes.
Néanmoins, les résultats des études sont assez contradictoires. En pratique, il est important de ne pas injecter un volume de plus de 1 mL afin de limiter le risque de déchirer la capsule articulaire. Il est recommandé de faire ces infiltrations sous contrôle scopique ou échographique pour s’assurer du positionnement intra-articulaire de l’aiguille.
En règle générale, on injecte 1/2 ml. Au delà l’injection distend la capsule et devient douloureuse. En effet, sans guidage ce type d’infiltration n’est effectivement intra-articulaire une fois sur deux. Une des rares études contrôlées des injections intra-articulaires de corticoïdes contre placebo dans la rhizarthrose a comparé 5 mg d’hexatrione à du sérum salé.
Le suivi était à 24 semaines et l’essai a inclus seulement 20 patients par groupe. Cette étude ne montre aucune différence entre l’injection placebo et l’injection du corticoïde. Pour autant, elle est critiquable en raison du faible nombre de patients inclus.
En dehors de l’injection de corticoïdes et en dehors de poussées, de nombreux essais ont étudié l’effet d’injection de l’acide hyaluronique. Beaucoup de ces études sont soit ouvertes, soit contrôlées contre un corticoïde.
Il est difficile de se faire une idée de l’efficacité de l’acide hyaluronique en raison de la variabilité de nombreux paramètres : nombre d’injections, type de l’acide hyaluronique utilisé, contrôle ou non de l’injection sous scopie, durée d’observation qui peut varier d’un à six mois.
Néanmoins, il ressort de ces études que l’acide hyaluronique est moins efficace que les corticoïdes sur une période courte, de deux à six semaines, mais supérieure aux corticoïdes au-delà de ce terme et ce jusqu’à une période pouvant aller jusqu’à six mois. L’efficacité de ces injections d’acide hyaluronique est surtout marquée sur la douleur, mais ne semble pas influencer la force de préhension.
L’étude la plus convaincante est une étude qui a comparé chez 60 patients deux injections à quinze jours d’intervalle soit d’acide hyaluronique, soit d’un placebo, soit d’un corticoïde pour une injection et d’un placebo pour la deuxième injection. L’évaluation s’est faite jusqu’à 26 semaines.
Les résultats de cette étude montrent l’absence de différence significative entre les groupes. Pour autant, l’analyse à quatre semaines montre que le corticoïde est supérieur à la réponse au placebo, 66 % versus 50 % et 44 % dans le groupe d’acide hyaluronique. À 26 semaines, l’acide hyaluronique a un pourcentage de répondeur supérieur, 68 % comparativement à 58 % pour le groupe corticoïde et 47 % pour le groupe placebo. Il n’est pas identifié de facteur prédictif de la réponse à ces injections d’acide hyaluronique.
De même, les indications et le nombre des infiltrations méritent d’être précisés par des études ultérieures. Néanmoins, dans la pratique courante, une arthrose débutante avec un stade 1 ou 2 dans la classification de Dell semble constituer une bonne indication de cette injection d’acide hyaluronique qui doit être au mieux réalisée sous contrôle soit scopique, soit par échographie.
Lorsque l’ensemble des éléments qui constituent l’arsenal thérapeutique médical est épuisé, que le niveau de la douleur et/ou du handicap fonctionnel reste important et au terme d’une évolution de plus de six mois, on peut avoir recours à la chirurgie.
Traitement chirurgical
L’idéal est la prévention de l’arthrose par la correction d’une dysplasie et qui peut faire appel avant la survenue de l’arthrose à une ostéotomie de réaxation articulaire. De même, la stabilisation d’un laxité trapézo-métacarpienne par ligamentoplastie est indiquée avant la décompensation arthrosique ou lorsqu’elle est encore toute débutante.
Au stade d’arthrose confirmé, les indications de dénervation trapézo-métacarpienne ou de ténotomie n’ont pratiquement plus cours. Reste trois indications chirurgicales : l’arthrodèse, la trapézectomie, et la prothèse, récemment réévalué dans le cadre d’une méta-analyse. L’arthrodèse est une intervention qui est quasiment abandonnée et mal évaluée dans la littérature.
En effet, elle visait à bloquer l’articulation trapézo-métacarpienne aux dépens d’une importante raideur de la colonne du pouce avec souvent une fusion difficile à obtenir (8 à 21 % de cas de non fusion). Son indication est devenue rare mais reste à discuter chez les travailleurs de force d’âge jeune.
Deux interventions chirurgicales sont donc à considérer : la trapézectomie ou la prothèse totale. Le préalable indispensable à la discussion chirurgicale est de savoir le nombre d’interlignes articulaires atteints sur un cliché de face. Dès lors que l’atteinte arthrosique déborde la seule l’articulation trapézo-métacarpienne, la prothèse n’est plus envisageable, car elle ne résoudrait pas le problème de douleurs des articulations arthrosiques adjacentes.
Dans ce cas de figure, seule l’indication de trapézectomie perdure. En cas d’une atteinte isolée de la trapézo-métacarpienne, le choix entre trapézectomie et prothèse dépend d’un certain nombre de critères : de l’âge du patient (en particulier l’âge de 70 ans ou plus est en faveur plutôt d’une prothèse), de la morphologie du trapèze, de l’importance de la déviation en adductus, du degré d’hyperextension de la MP.
Trapézectomie
La trapézectomie consiste en l’ablation du trapèze, elle peut être totale ou partielle, elle peut être associée à l’interposition soit d’un tendon, soit d’un cartilage souvent costal, soit de différents matériaux soit synthétiques soit d’implants de silicone, voire d’un implant de pyro-carbone.
Les implants en silicone ont provoqué des siliconites de l’ensemble du carpe parfois sévère et sont totalement abandonnés. Il n’y a pas de certitude que l’interposition d’un matériel ou la reconstruction ligamentaire donnent des résultats supérieurs à la seule trapézectomie. La surveillance évolutive de cette intervention est radiographique.
On mesure la distance de l’espace vide qui tend à diminuer au fil du temps, on recherche la présence d’ossifications et la possibilité d’une ostéolyse de voisinage. Les avantages de la trapézectomie sont sa relative innocuité et de conserver la mobilité du pouce au prix d’une force qui est modérément diminuée et reste stable.
Cette intervention présente moins de risque infectieux si l’on y associe pas une interposition prothétique. La reprise de fonction est possible à la sixième semaine et le résultat optimum obtenu en quatre à six mois et ainsi deux fois plus long à obtenir que pour la prothèse.
Cette intervention ne corrige pas la déformation de la colonne du pouce. La trapézectomie est l’intervention idéale chez un patient de moins de 70 ans, encore actif qui va solliciter pendant de nombreuses années sa pince pouce-index.
La prothèse
Il existe plusieurs variétés de prothèse totale de l’articulation trapézo-métacarpienne. La plus fréquemment posée est une prothèse scellée de type Guépar. Mais, il existe de nombreuses autres variantes, comme les prothèses sphéroïde inversés, des prothèses non cimentées ou des prothèses sphéroïdes hybrides. L’indication de prothèse nécessite une atteinte isolée de la trapézo-métacarpienne, un trapèze suffisamment large et non détruit pour recevoir la partie prothétique trapézienne, l’absence de rétraction de la première commissure, l’absence d’atteinte de la MP en hyper extension.
L’indication idéale de la prothèse est un patient âgé de 70 ou plus qui n’imposera pas de contraintes importantes sur la prothèse par l’utilisation d’une force importante de la pince pouce/index. La force obtenue est sinon identique à celle de la trapézectomie et la correction de la déformation meilleure L’avantage est une récupération rapide et un résultat optimum obtenu en deux mois avec une reprise de fonction obtenu en trois semaines.
La principale complication la prothèse est le risque de luxation qui peut être précoce et de descellement observé dans 15 % des cas et qui est généralement tardif soulignant la prudence qu’il y a à proposer cette intervention plutôt aux patients âgés.
Dans tous les cas, l’intervention chirurgicale n’est pas adaptée aux déformations en pouces adductus évolués ou fixés qui sont au demeurant généralement devenues peu douloureux et surtout invalidants par la déformation plus que par la douleur.
Enfin, la rhizarthrose est d’une affection très fréquente, volontiers bilatérale, prédominant sur la main dominante et touchant plus souvent les femmes. Son évolution naturelle est marquée par une diminution des douleurs souvent après plusieurs années d’évolution, au prix d’une déformation plus ou moins importante, et plus ou moins handicapante. Sa prise en charge est essentiellement médicale.
Elle vise à réduire les douleurs et à maintenir la mobilité de l’articulation de la colonne du pouce. On peut avoir recours à des infiltrations locales. Il ne faudra pas négliger la possibilité de recourir à une chirurgie qui donne en règle générale de très bons résultats, notamment la trapézectomie chez des patients encore jeunes.
| Références : Revue du Rhumatisme Monographies Xavier Chevalier. a, Christian Compaore. a, Florent Eymard. a, René-Marc Flipo. b a. Service de rhumatologie, hôpital Henri-Mondor. b. Service de rhumatologie, centre Verhaegen, hôpital Roger-Salengro, CHU de Lille. |